Zusammenfassung
Abstract
Inhalt
1 Einleitung
2 Material und Methoden
3 Ergebnisse
4 Diskussion
4.1 Baumkronen als Lebensraum gefährdeter Arten
4.2 Bewertung der Baumkronenbenebelungsmethode
5 Ausblick – Möglichkeiten der Baumkronenbenebelung
Zusatzmaterial zum Beitrag
Dank
1 Einleitung
2 Material und Methoden
Gewöhnliche Esche (Fraxinus excelsior
Rot-Esche (F. pennsylvanica
Stieleiche (Quercus robur
Flatterulme (Ulmus laevis
Winterlinde (Tilia cordata
ein Exemplar der Wildbirne (Pyrus pyraster
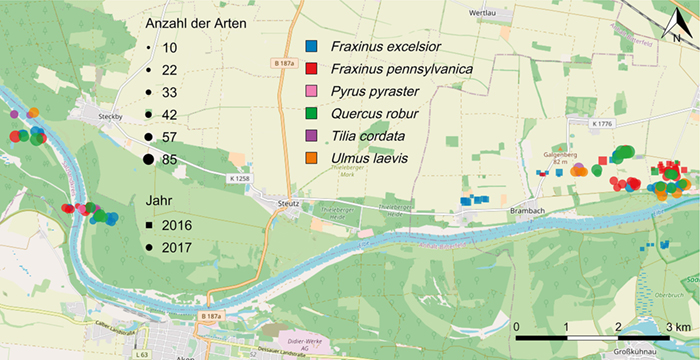
|
Tab. 1: Mittels Fogging (Vernebelung) nachgewiesene Käferarten der untersuchten Baumarten über alle Jahre und getrennt für die Jahre 2016 und 2017.
Table 1: Fogged beetle species of the investigated tree species detected across all years and separately for the years 2016 and 2017.
|
|||||||
|
2016 – 2017
|
Gesamt
|
Fraxinus excelsior
|
Fraxinus pennsylvanica
|
Quercus robur
|
Ulmus laevis
|
Tilia cordata
|
Pyrus pyraster
|
|
Anzahl der Benebelungen
|
149
|
57
|
50
|
23
|
12
|
6
|
1
|
|
Anzahl der Arten
|
602
|
421
|
338
|
317
|
215
|
131
|
39
|
|
Anzahl der Individuen
|
30 458
|
5 476
|
7 363
|
7 846
|
8 298
|
1 360
|
115
|
|
465
|
313
|
262
|
248
|
173
|
101
|
28
|
|
|
Davon RL-Arten2
|
108
|
61
|
54
|
65
|
37
|
21
|
6
|
|
Anteil von RL-Arten2 (%)
|
23,23
|
19,49
|
20,61
|
26,21
|
21,39
|
20,79
|
21,43
|
|
23 509
|
3 603
|
5 000
|
6 128
|
7 863
|
852
|
63
|
|
|
Davon Individuen von RL-Arten2
|
2 889
|
665
|
654
|
1 085
|
333
|
138
|
14
|
|
Anteil der Individuen von RL-Arten2 (%)
|
12,29
|
18,46
|
13,08
|
17,71
|
4,24
|
16,20
|
22,22
|
|
2017
|
Gesamt
|
Fraxinus excelsior
|
Fraxinus pennsylvanica
|
Quercus robur
|
Ulmus laevis
|
Tilia cordata
|
Pyrus pyraster
|
|
Anzahl der Benebelungen
|
100
|
30
|
30
|
21
|
12
|
6
|
1
|
|
Anzahl der Arten
|
521
|
337
|
279
|
305
|
215
|
131
|
39
|
|
Anzahl der Individuen
|
25 976
|
3 584
|
5 228
|
7 391
|
8 298
|
1 360
|
115
|
|
401
|
248
|
214
|
238
|
173
|
101
|
28
|
|
|
Davon RL-Arten2
|
99
|
55
|
41
|
63
|
37
|
21
|
6
|
|
Anteil von RL-Arten2 (%)
|
24,69
|
22,18
|
19,16
|
26,47
|
21,39
|
20,79
|
21,43
|
|
20 714
|
2 252
|
3 918
|
5 766
|
7 863
|
852
|
63
|
|
|
Davon Individuen von RL-Arten2
|
2 420
|
473
|
439
|
1 023
|
333
|
138
|
14
|
|
Anteil der Individuen von RL-Arten2 (%)
|
11,68
|
21,00
|
11,20
|
17,74
|
4,24
|
16,20
|
22,22
|
|
2016
|
Gesamt
|
Fraxinus excelsior
|
Fraxinus pennsylvanica
|
Quercus robur
|
|
|
|
|
|
49
|
27
|
20
|
2
|
|
|
|
|
|
303
|
235
|
171
|
65
|
|
|
|
|
|
4 482
|
1 892
|
2 135
|
455
|
|
|
|
|
|
227
|
172
|
131
|
52
|
|
|
|
|
|
36
|
24
|
28
|
12
|
|
|
|
|
|
15,86
|
13,95
|
21,37
|
23,08
|
|
|
|
|
|
2 795
|
1 351
|
1 082
|
362
|
|
|
|
|
|
469
|
192
|
215
|
62
|
|
|
|
|
|
16,78
|
14,21
|
19,87
|
17,13
|
|
|
|
|
1 Arten, die in den Roten Listen Sachsen-Anhalt (LAU 2020) aufgeführt werden
2 Arten der Gefährdungskategorien 1, 2, 3, R der Roten Listen Sachsen-Anhalt (LAU 2020) sowie der Neu- und Wiederfunde
|
|||||||
|
Tab. 2: Kategorien der Roten Listen Sachsen-Anhalt (LAU 2020).
Table 2: Categories of the Red Lists of Saxony-Anhalt (LAU 2020).
|
|
|
Rote-Liste-Kategorie
|
|
|
0
|
Ausgestorben oder verschollen
|
|
R
|
Extrem seltene Arten mit geographischer Restriktion
|
|
1
|
Vom Aussterben bedroht
|
|
2
|
Stark gefährdet
|
|
3
|
Gefährdet
|
|
G
|
Gefährdung anzunehmen, aber Status unbekannt
|
|
D
|
Daten defizitär
|
|
V
|
Arten der Vorwarnliste
|
|
*
|
Ungefährdet
|
|
Fett = im Projekt berücksichtigte Rote-Liste-Kategorien
|
|
3 Ergebnisse
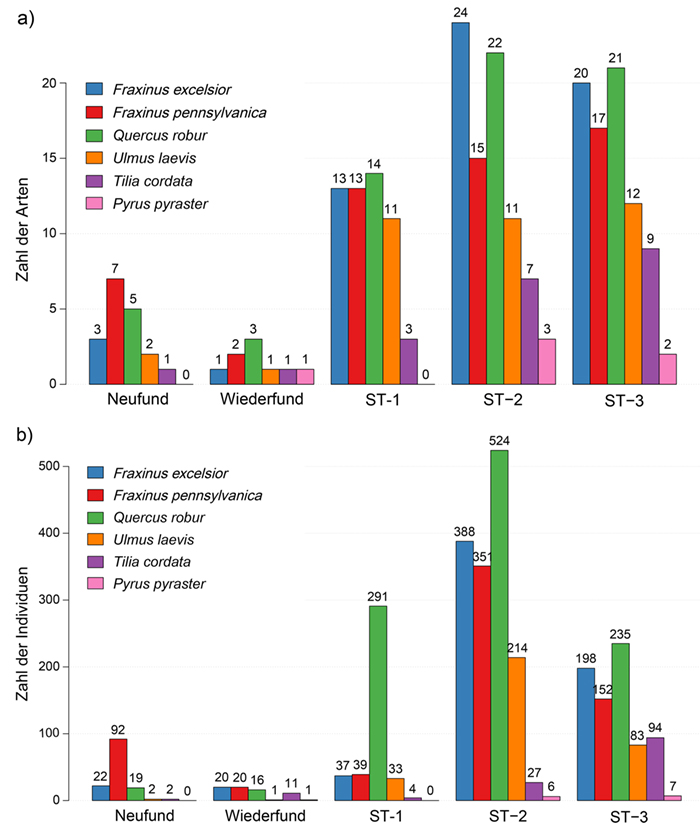
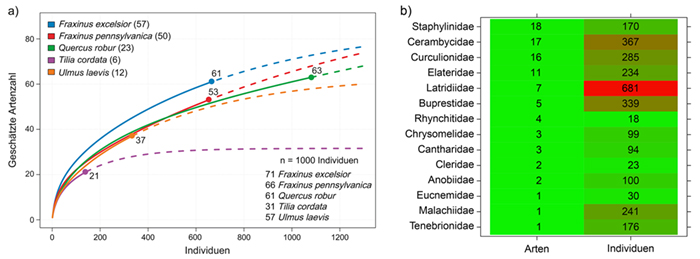
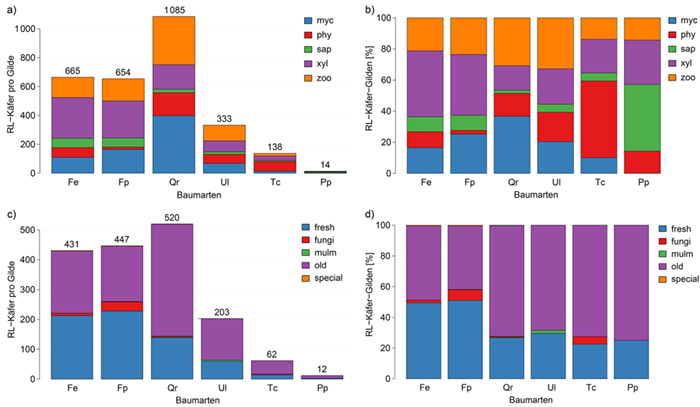
4 Diskussion
4.1 Baumkronen als Lebensraum gefährdeter Arten
4.2 Bewertung der Baumkronenbenebelungsmethode
5 Ausblick – Möglichkeiten der Baumkronenbenebelung
Zusatzmaterial zum Beitrag
Floren A., Sprick P., Horchler P.J., Müller T. (2021): Baumkronen als Habitat gefährdeter Käfer am Beispiel von Hartholzauwäldern in Sachsen-Anhalt, Region Mittelelbe. Natur und Landschaft 96(11): 509 – 516. DOI: 10.19217/NuL2021-11-01
Gesamt-PDF
● Zusatzmaterial (Abb. A, Tab. A) im Heftlayout als Gesamt-PDF herunterladen
6 Literatur
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑
↑

